Kardiotoksyczność w onkologii
1. Czym jest kardiotoksyczność?
Kardiotoksyczność to ogół niekorzystnych działań leczenia onkologicznego (chemioterapii, radioterapii, immunoterapii) na układ sercowo-naczyniowy. Może prowadzić do uszkodzenia mięśnia sercowego, naczyń krwionośnych i zaburzeń rytmu serca.
Występuje częściej u pacjentów:
-
leczonych na nowotwory piersi, płuc i chłoniaki śródpiersia,
-
otrzymujących antracykliny (np. doksorubicynę), trastuzumab czy inhibitory kinaz,
-
poddawanych radioterapii w obrębie klatki piersiowej (szczególnie lewej strony).
2. Mechanizmy uszkodzeń serca
-
Chemioterapia – stres oksydacyjny, uszkodzenia mitochondriów, martwica kardiomiocytów.
-
Radioterapia – włóknienie mięśnia sercowego, zapalenie osierdzia, zwężenie naczyń wieńcowych.
-
Immunoterapia – reakcje autoimmunologiczne, zapalenie mięśnia sercowego.
3. Objawy kardiotoksyczności
-
duszność, obrzęki, ograniczona tolerancja wysiłku,
-
bóle w klatce piersiowej, zaburzenia rytmu, omdlenia,
-
objawy niewydolności serca (obniżona frakcja wyrzutowa w echokardiografii).
4. Choroby wywołane kardiotoksycznością
-
kardiomiopatia i niewydolność serca,
-
choroba wieńcowa (uszkodzenie tętnic wieńcowych),
-
zaburzenia rytmu (arytmie, migotanie przedsionków),
-
choroby zastawek serca (zwłóknienie, zwężenia),
-
zapalenie osierdzia i wsierdzia.
5. Diagnostyka i monitoring
-
EKG – podstawowa kontrola rytmu.
-
Echokardiografia (echo serca) – ocena frakcji wyrzutowej (LVEF).
-
Biomarkery – troponiny, BNP/NT-proBNP (wczesne wykrywanie uszkodzeń).
-
MRI serca – ocena włóknienia i funkcji mięśnia sercowego.
6. Jak zmniejszyć ryzyko kardiotoksyczności?
-
Planowanie radioterapii – IMRT, VMAT, protonoterapia, technika DIBH (głęboki wdech przy napromienianiu lewej piersi).
-
Zmniejszenie dawek leków kardiotoksycznych – np. liposomalna doksorubicyna.
-
Profilaktyka farmakologiczna – ACE-inhibitory, beta-blokery, statyny.
-
Kardiomonitoring w trakcie terapii – regularne EKG i echo.
-
Kardioonkologia – współpraca kardiologa i onkologa od momentu planowania leczenia.
7. Leczenie powikłań
-
standardowe leczenie niewydolności serca (ACE-I, beta-blokery, diuretyki),
-
zabiegi interwencyjne (np. angioplastyka w chorobie wieńcowej),
-
leczenie arytmii (farmakologiczne lub urządzenia: ICD, stymulator).
8. Znaczenie w praktyce klinicznej
Kardiotoksyczność to rosnący problem w onkologii, bo coraz więcej pacjentów przeżywa nowotwory i żyje długo po leczeniu. Długofalowe uszkodzenia serca stają się więc nowym wyzwaniem medycyny, a kardioonkologia rozwija się jako odrębna dziedzina, łącząca onkologię, kardiologię i diagnostykę obrazową.
IMRT – Intensity Modulated Radiotherapy
1. Czym jest IMRT?
IMRT (Radioterapia z modulowaną intensywnością wiązki) to technika napromieniania, w której kształt i intensywność promieniowania są precyzyjnie modulowane za pomocą systemu listków kolimatora (MLC – Multi-Leaf Collimator).
👉 Dzięki temu można podać wysoką dawkę w obręb guza, jednocześnie oszczędzając zdrowe tkanki i narządy krytyczne (OAR – Organs At Risk).
2. Zasada działania
-
Akcelerator liniowy wytwarza wiązkę fotonów.
-
Kolimator (MLC) składający się z wielu ruchomych listków reguluje kształt i intensywność wiązki.
-
Planowanie odbywa się komputerowo (tzw. inverse planning – lekarz i fizyk definiują dawkę w guzie i maksymalne dopuszczalne dla otoczenia, a system optymalizuje kształt pól).
3. Urządzenia i producenci
-
Varian (Eclipse, TrueBeam, Halcyon)
-
Elekta (Versa HD, Monaco)
-
Siemens (Artiste, ONCOR)
-
Accuray (TomoTherapy, Radixact)
4. Zastosowania kliniczne
-
nowotwory głowy i szyi,
-
nowotwory prostaty,
-
rak piersi (zwłaszcza lewostronny – blisko serca),
-
rak płuca,
-
chłoniaki śródpiersia.
5. Dawki i frakcjonowanie
-
Standard: 1,8–2 Gy / frakcję, 5x w tygodniu, do całkowitej dawki 50–70 Gy.
-
Możliwość stosowania hipofrakcjonowania (większe dawki w mniejszej liczbie frakcji).
6. Zalety IMRT
-
bardzo precyzyjne dopasowanie rozkładu dawki do kształtu guza,
-
redukcja dawek dla narządów krytycznych (np. serca, płuc, rdzenia kręgowego),
-
możliwość leczenia guzów złożonych anatomicznie,
-
mniejsze ryzyko powikłań i kardiotoksyczności (np. przy raku piersi).
7. Ograniczenia i wyzwania
-
dłuższy czas planowania i napromieniania niż w konwencjonalnej radioterapii,
-
większa złożoność – wymaga doświadczonego zespołu (lekarz, fizyk, technik),
-
wyższe koszty, szczególnie w porównaniu do 2D/3D RT,
-
ryzyko błędów przy nieprawidłowym planowaniu (konieczność QA – kontroli jakości).
8. Kontrola jakości (QA – Quality Assurance)
-
weryfikacja planu dawki przed rozpoczęciem leczenia,
-
pomiary fantomowe (czy rozkład dawki zgadza się z planem),
-
codzienna kontrola akceleratora (kalibracja, testy MLC),
-
audyty międzynarodowe (np. IAEA, ESTRO).
✅ IMRT jest obecnie złotym standardem w wielu typach nowotworów i stanowi krok pośredni między klasyczną radioterapią 3D a protonoterapią.
Jak IMRT zmniejsza ryzyko kardiotoksyczności?
1. Precyzyjne kształtowanie dawki
-
Dzięki kolimatorowi MLC IMRT pozwala podać większą dawkę w obrębie guza, a jednocześnie „wycinać” pole napromieniania tak, aby serce i duże naczynia otrzymywały możliwie małą dawkę rozproszoną.
-
W klasycznej 3D radioterapii serce dostawało wyższą „przygodną” dawkę – IMRT redukuje to ryzyko.
2. Ochrona narządów krytycznych (OAR – Organs At Risk)
W planowaniu IMRT lekarz i fizyk ustalają limity dawki dla serca, płuc i przełyku. System komputerowy oblicza taki rozkład, by:
-
guz dostał np. 60–70 Gy,
-
serce <5–10 Gy (w zależności od wytycznych),
-
duże naczynia i płuca także w bezpiecznym zakresie.
3. Radioterapia raka piersi (szczególnie lewej)
-
Klasyczna radioterapia często obejmowała fragment serca.
-
IMRT (a także VMAT) pozwala:
-
„owinąć się” dawką wokół serca,
-
zastosować technikę DIBH (Deep Inspiration Breath Hold) – pacjentka wstrzymuje oddech na wdechu, a serce oddala się od piersi → jeszcze mniejsze dawki dla mięśnia sercowego i tętnic wieńcowych.
-
4. Radioterapia chłoniaków śródpiersia i raka płuca
-
U pacjentów młodych, którzy przeżyją wiele lat, kardiotoksyczność może ujawnić się po 10–20 latach.
-
IMRT ogranicza dawkę dla serca i aorty, zmniejszając ryzyko choroby wieńcowej i kardiomiopatii popromiennej.
5. Dane kliniczne
-
Badania pokazują, że zastosowanie IMRT zamiast 3D-CRT obniża średnią dawkę dla serca nawet o 30–50%.
-
To przekłada się na mniejsze ryzyko:
-
niewydolności serca,
-
choroby wieńcowej,
-
arytmii popromiennych.
-
6. Uzupełnienie – kardioonkologia
-
IMRT + monitorowanie kardiologiczne (echo, EKG, biomarkery) = zmniejszenie powikłań sercowych.
-
Współpraca radioterapeuty i kardiologa pozwala dobrać optymalny plan i szybko reagować na wczesne objawy uszkodzenia serca.
✅ Podsumowując: IMRT zmniejsza kardiotoksyczność, bo pozwala zminimalizować dawkę dla serca i naczyń przy zachowaniu pełnej dawki w guzie – a dodatkowo daje możliwość stosowania technik oddechowych (DIBH), które jeszcze bardziej chronią serce.
Techniki radioterapii zmniejszające kardiotoksyczność
1. VMAT – Volumetric Modulated Arc Therapy
-
Zasada: rozwinięcie IMRT – akcelerator obraca się wokół pacjenta i w czasie rzeczywistym zmienia intensywność, kształt wiązki i prędkość obrotu.
-
Zalety:
-
krótszy czas napromieniania niż IMRT (zamiast kilkunastu pól → 1–2 łuki),
-
jeszcze lepsze dopasowanie dawki do kształtu guza,
-
mniejsza dawka dla serca i płuc.
-
-
W kontekście kardiotoksyczności:
-
stosowana w nowotworach piersi, płuca i chłoniakach śródpiersia,
-
badania pokazują zmniejszenie średniej dawki dla serca o 20–40% w porównaniu do 3D-CRT.
-
2. Protonoterapia
-
Zasada: wykorzystuje wiązki protonów, które oddają energię głównie w tzw. piku Bragga – maksymalna dawka w guzie, a poza nim praktycznie brak promieniowania.
-
Zalety:
-
bardzo mała dawka poza celem,
-
najlepsza ochrona narządów krytycznych (OAR),
-
szczególnie polecana w leczeniu dzieci i młodych dorosłych (aby ograniczyć późne powikłania sercowe).
-
-
W kontekście kardiotoksyczności:
-
radykalnie zmniejsza dawkę dla serca w raku piersi i chłoniakach śródpiersia,
-
redukuje ryzyko choroby wieńcowej i kardiomiopatii popromiennej.
-
3. DIBH – Deep Inspiration Breath Hold
-
Zasada: pacjentka wstrzymuje oddech przy głębokim wdechu podczas napromieniania piersi.
-
Efekt: płuca się rozszerzają, a serce „cofa” się od klatki piersiowej → większa odległość od pola napromieniania.
-
Zalety:
-
technika prosta i tania (wymaga tylko systemu kontroli oddechu),
-
szczególnie skuteczna w raku lewej piersi,
-
zmniejsza średnią dawkę dla serca nawet o 50%.
-
Podsumowanie – wpływ na kardiotoksyczność
| Technika | Mechanizm ochrony | Redukcja dawki dla serca | Zastosowania |
|---|---|---|---|
| IMRT | modulacja intensywności, kształtowanie dawki | 30–50% w stosunku do 3D-CRT | głowa-szyja, pierś, płuca, chłoniaki |
| VMAT | modulacja podczas obrotu akceleratora | 20–40% względem 3D-CRT | piersi, płuca, guzy miednicy |
| Protonoterapia | pik Bragga – brak dawki poza guzem | >70% w porównaniu z fotonami | piersi, chłoniaki, dzieci, młodzi dorośli |
| DIBH | oddech odsuwa serce od pola | do 50% redukcji | rak lewej piersi |
✅ W praktyce klinicznej:
-
IMRT i VMAT to standard w wielu ośrodkach,
-
DIBH jest szeroko stosowane u kobiet z rakiem lewej piersi,
-
Protonoterapia – najlepsza pod względem ochrony serca, ale dostępna tylko w kilku ośrodkach w Polsce i Europie ze względu na koszty.
-
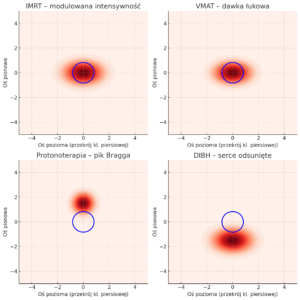
🔴 Czerwone pola – rozkład dawki promieniowania,
-
🔵 Niebieski kontur – guz.
➡️ IMRT – dopasowana dawka, mniejsze obciążenie serca.
➡️ VMAT – podobnie jak IMRT, ale szybciej i w formie łuku.
➡️ Protonoterapia – bardzo precyzyjny pik Bragga, prawie brak dawki poza guzem.
➡️ DIBH – dzięki głębokiemu wdechowi serce „odsuwa się” od pola napromieniania.
| Technika | Mechanizm działania | Zalety | Ograniczenia | Wpływ na kardiotoksyczność |
|---|---|---|---|---|
| IMRT (Intensity Modulated Radiotherapy) | modulacja intensywności wiązki za pomocą kolimatora MLC, wiele pól napromieniania | bardzo dobre dopasowanie dawki, oszczędzanie serca i płuc | dłuższy czas planowania i napromieniania, wyższe koszty | redukcja średniej dawki dla serca o 30–50% względem 3D-CRT |
| VMAT (Volumetric Modulated Arc Therapy) | modulacja dawki w czasie obrotu akceleratora wokół pacjenta | krótszy czas leczenia niż IMRT, dobra ochrona narządów krytycznych | większa złożoność QA, wyższe wymagania sprzętowe | redukcja średniej dawki dla serca o 20–40% |
| Protonoterapia | wykorzystanie piku Bragga – maksymalna dawka w guzie, minimalna poza nim | najlepsza ochrona serca i płuc, szczególnie u dzieci i młodych dorosłych | bardzo wysokie koszty, ograniczona dostępność ośrodków | redukcja dawki dla serca >70% w porównaniu do fotonów |
| DIBH (Deep Inspiration Breath Hold) | pacjent wstrzymuje oddech w głębokim wdechu → serce oddala się od piersi | prosta, tania, bardzo skuteczna w raku lewej piersi | wymaga współpracy pacjenta, nie dla wszystkich możliwa | zmniejszenie średniej dawki dla serca nawet o 50% |
| Technika | Średnia dawka do serca (Dmean) – typowo | V25 / V30 serca – typowo lub zalecenia | Uwagi kliniczne |
|---|---|---|---|
| IMRT | ~3–6 Gy przy piersi lewej, zwykle niżej niż 3D-CRT. (pmc.ncbi.nlm.nih.gov) | V25 < 10% jako punkt odniesienia (QUANTEC); w badaniach V30 ok. 3–9%. (pmc.ncbi.nlm.nih.gov) | Precyzyjne oszczędzanie OAR; wymagany QA. (pmc.ncbi.nlm.nih.gov) |
| VMAT | ~4–7 Gy (zależnie od planu); zwykle niżej niż 3D-CRT, porównywalnie do IMRT. (eurjbreasthealth.com) | V25/V30 często mniejsze niż w 3D-CRT; przykładowo V30 niższe vs IMRT w jednym z porównań. (pmc.ncbi.nlm.nih.gov) | Krótszy czas napromieniania; złożony QA. (pmc.ncbi.nlm.nih.gov) |
| Protonoterapia | ~0.3–1.0 Gy (median Dmean ~0.5 Gy w seriach klinicznych). (pmc.ncbi.nlm.nih.gov) | V25 zwykle ~0–5%; w protokołach często cel: Dmean ≤ 4 Gy, V25 < 5%. (sciencedirect.com) | Największe oszczędzanie serca (pik Bragga), ale ograniczona dostępność. (pmc.ncbi.nlm.nih.gov) |
| DIBH (technika oddechowa) | Redukcja Dmean o ~1–3.5 Gy vs. free-breathing; przykładowo z ~2.6 Gy do ~1.4 Gy lub o ~3.4 Gy. (iv.iiarjournals.org) | V25/V30 istotnie mniejsze vs. free-breathing (np. spadek V25 i V30 w DIBH). (journals.lww.com) | Tania i skuteczna metoda ochrony serca, szczególnie w piersi lewej. (pmc.ncbi.nlm.nih.gov) |