Neurofibromatoza
NF1 (Neurofibromatoza typu 1, choroba von Recklinghausena)
-
Gen: mutacja w genie NF1 na chromosomie 17 → koduje białko neurofibrominę (działa jak supresor nowotworowy).
-
Objawy:
-
plamy „café-au-lait” na skórze,
-
piegi w okolicach pachwin i pach,
-
liczne nerwiaki (neurofibroma),
-
guzki Lischa (małe zmiany w tęczówce),
-
możliwe guzy OUN (np. glejaki nerwu wzrokowego),
-
deformacje kostne (skolioza, dysplazje).
-
-
Dziedziczenie: autosomalnie dominujące, duża zmienność objawów nawet w tej samej rodzinie.
-
Częstość: 1 na ok. 3000 urodzeń.
NF2 (Neurofibromatoza typu 2)
-
Gen: mutacja w genie NF2 na chromosomie 22 → koduje merlinę (schwannominę).
-
Objawy:
-
obustronne schwannoma nerwu VIII (nerwu słuchowego) → postępująca głuchota, szumy uszne, zaburzenia równowagi,
-
inne guzy OUN (meningioma, ependymoma),
-
zmiany oczne (zaćma podtorebkowa tylna).
-
-
Częstość: rzadsza niż NF1 (ok. 1:25 000).
-
Dziedziczenie: autosomalne dominujące.
NF3
Tu jest mały haczyk 🙂
-
NF3 w klasycznej medycynie nie istnieje jako odrębna jednostka.
-
W starszej literaturze albo niektórych źródłach można spotkać określenia typu neurofibromatoza typu 3, ale zazwyczaj:
-
chodzi o schwannomatozę (uznawaną dziś za trzecią główną postać z grupy fakomatoz pokrewnych NF1/NF2),
-
albo o inne warianty mozaikowe.
-
-
Schwannomatoza charakteryzuje się mnogimi guzami osłonek nerwów (schwannoma), ale bez typowych objawów NF2 (czyli brak obustronnych guzów nerwu VIII).
👉 Podsumowując:
-
NF1 = plamy café-au-lait + neurofibroma + guzy OUN
-
NF2 = guzy nerwu słuchowego + meningioma/ependymoma
-
NF3 = schwannomatoza (rzadsza, kontrowersyjna klasyfikacja).
🧬 Neurofibromatoza – trzy przykłady kliniczne
1. NF1 (choroba von Recklinghausena)
Pacjent: 12-letni chłopiec
Objawy początkowe: liczne plamy café-au-lait widoczne od wczesnego dzieciństwa, piegi w okolicach pachowych.
Przebieg: w wieku 10 lat pojawiły się miękkie guzki podskórne (neurofibroma skórne), a w badaniu okulistycznym – guzki Lischa w tęczówce.
Badania: rezonans magnetyczny głowy wykazał glioma nerwu wzrokowego.
Postępowanie: obserwacja okulistyczna, konsultacje neurologiczne, wsparcie psychologiczne.
Uwagi: typowy obraz NF1 – zmiany skórne, guzy nerwów i ryzyko powikłań ocznych/neurologicznych.
2. NF2 (neurofibromatoza typu 2)
Pacjent: 28-letnia kobieta, studentka
Objawy początkowe: postępujące pogorszenie słuchu i szumy uszne w wieku 24 lat.
Przebieg: MRI wykazało obustronne guzy kąta mostowo-móżdżkowego (schwannoma nerwu VIII).
Objawy towarzyszące: zaburzenia równowagi, sporadyczne parestezje w kończynach.
Postępowanie: operacyjne usunięcie jednego guza, implant słuchowy typu ABI (auditory brainstem implant).
Uwagi: klasyczny przypadek NF2 – obustronne schwannomy nerwu słuchowego, prowadzące do głuchoty.
3. Schwannomatoza (NF3)
Pacjent: 45-letni mężczyzna
Objawy początkowe: przewlekłe bóle kończyn od kilku lat, bez wyraźnych zmian skórnych.
Przebieg: badanie MRI wykazało liczne guzy osłonek nerwów obwodowych (schwannoma) na kończynach i tułowiu, brak zajęcia nerwu słuchowego.
Objawy: ból neuropatyczny oporny na klasyczne leki przeciwbólowe.
Postępowanie: leczenie operacyjne wybranych guzów, farmakoterapia bólu (gabapentyna, pregabalina), fizjoterapia.
Uwagi: schwannomatoza odróżnia się od NF2 brakiem guzów nerwu słuchowego i dominującymi dolegliwościami bólowymi.
✅ Te trzy przypadki dobrze pokazują różnice:
-
NF1 → skóra + guzy nerwów + objawy okulistyczne
-
NF2 → guzy nerwu VIII, zaburzenia słuchu/równowagi
-
NF3 → liczne schwannomy, głównie ból jako dominujący objaw
🔹 Co to są bramki DNA?
To układy logiczne zbudowane z cząsteczek DNA (lub RNA), które działają podobnie jak klasyczne bramki logiczne w elektronice (AND, OR, NOT, NAND, NOR, XOR…).
-
Wejściem są zwykle cząsteczki DNA (np. krótkie oligonukleotydy, które mogą się do siebie przyłączać).
-
Wyjściem jest reakcja biochemiczna: np. uwolnienie innego fragmentu DNA, emisja fluorescencji, zmiana struktury.
🔹 Jak to działa w praktyce?
-
Komplementarność zasad – sekwencja A-T i G-C działa jak „dopasowanie wtyczki do gniazdka”.
-
Strand displacement – jedna nić DNA może wypierać inną, jeśli ma lepsze dopasowanie – to mechanizm używany jako przełącznik.
-
Reakcje enzymatyczne – np. polimerazy, nukleazy, ligazy – mogą pełnić funkcję przetwarzania sygnału.
🔹 Przykłady bramek DNA
-
AND: wyjście pojawia się tylko wtedy, gdy obecne są dwa różne oligonukleotydy wejściowe.
-
OR: wyjście pojawia się, gdy obecny jest przynajmniej jeden wejściowy fragment.
-
NOT: brak wyjścia, jeśli pojawi się określony inhibitor (np. nić komplementarna).
-
NAND/NOR: kombinacje powyższych.
🔹 Zastosowania
-
Biokomputery – działające w probówce (Adleman 1994: rozwiązanie problemu ścieżki Hamiltona przy użyciu DNA).
-
Diagnostyka medyczna – bramki DNA wykrywają kombinacje markerów genetycznych i dają sygnał (np. fluorescencję).
-
Terapie celowane – koncepcja „smart drugs”: lek aktywuje się tylko w obecności specyficznych sekwencji DNA/RNA (np. w komórkach nowotworowych).
-
Nanotechnologia – programowanie nanostruktur DNA (DNA origami) z logiką.
bramki DNA mogą być użyte w diagnostyce NF1/NF2/NF3?
Teoretycznie tak, praktycznie – jeszcze nie w rutynie klinicznej, ale w laboratoriach badawczych takie podejścia już są rozwijane.
1. Jak działałaby taka diagnostyka?
Zamiast klasycznego PCR/sekwencjonowania można zaprojektować biosensory DNA/RNA w formie bramek logicznych:
-
Wejście A: obecność mutacji w genie NF1 (np. konkretne „junction” w mRNA).
-
Wejście B: marker nadaktywnego szlaku RAS/MAPK (typowy dla NF1).
-
Wejście C: marker komórek Schwanna (NF2/NF3).
-
Wejście D (NOT): sekwencja kontrolna ze zdrowych tkanek.
Brama typu A AND B AND C AND NOT D uruchomiłaby sygnał (np. fluorescencję), tylko jeśli pacjent ma charakterystyczny profil NF.
2. Technologie możliwe do wykorzystania
-
Toehold switches (RNA) → mogą świecić fluorescencyjnie, gdy obecna jest konkretna sekwencja RNA.
-
DNA strand displacement → kaskady oligonukleotydów, które dają sygnał tylko przy odpowiedniej kombinacji wejść.
-
CRISPR-dCas12/13 → enzymy wykrywające RNA/DNA, mogą emitować sygnał fluorescencji po cięciu „reportera”.
3. Zalety w NF
-
Wielokryterialność: można od razu odróżnić NF1 od NF2 i schwannomatozy (NF3), bo każda ma inne sekwencje-geny docelowe.
-
Szybkość: test w probówce zamiast pełnego sekwencjonowania → taniej i szybciej.
-
Czułość: bramki DNA potrafią wykrywać pojedyncze kopie RNA.
4. Ograniczenia
-
Standaryzacja: każdy pacjent z NF1/NF2 może mieć inną mutację – więc trzeba by budować panele bramek.
-
Mozaikowatość: niektóre mutacje NF1 występują tylko w części komórek → bramka mogłaby przeoczyć wynik.
-
Praktyka kliniczna: dziś złotym standardem jest sekwencjonowanie (NGS, panel genów).
👉 Podsumowując:
Bramki DNA mogłyby być użyte jako biosensory do szybkiego screeningu NF, np. z krwi lub wymazu, ale obecnie stosuje się je tylko w eksperymentach. Najbliżej praktyki są CRISPR-diagnostyki (SHERLOCK, DETECTR), które działają jak „biologiczne bramki logiczne” i mogłyby być przeprojektowane na NF.
Założone „wejścia” (biosensory)
-
A_NF1 – patogenna mutacja NF1 (panel sond specyficznych / junction RNA).
-
B_RAS – sygnatura nadaktywnego RAS/MAPK (np. transkrypty: DUSP6, ETV4/5).
-
C_SCH – marker linii Schwanna (np. SOX10, NGFR/p75) – przydatny przy materiałach z guzów.
-
E_NF2 – patogenna mutacja NF2.
-
F_YAP – sygnatura aktywności YAP/TAZ (np. CTGF, CYR61) – typowe dla utraty merliny.
-
G_SMARCB1 – mutacja / utrata INI1.
-
H_LZTR1 – mutacja LZTR1.
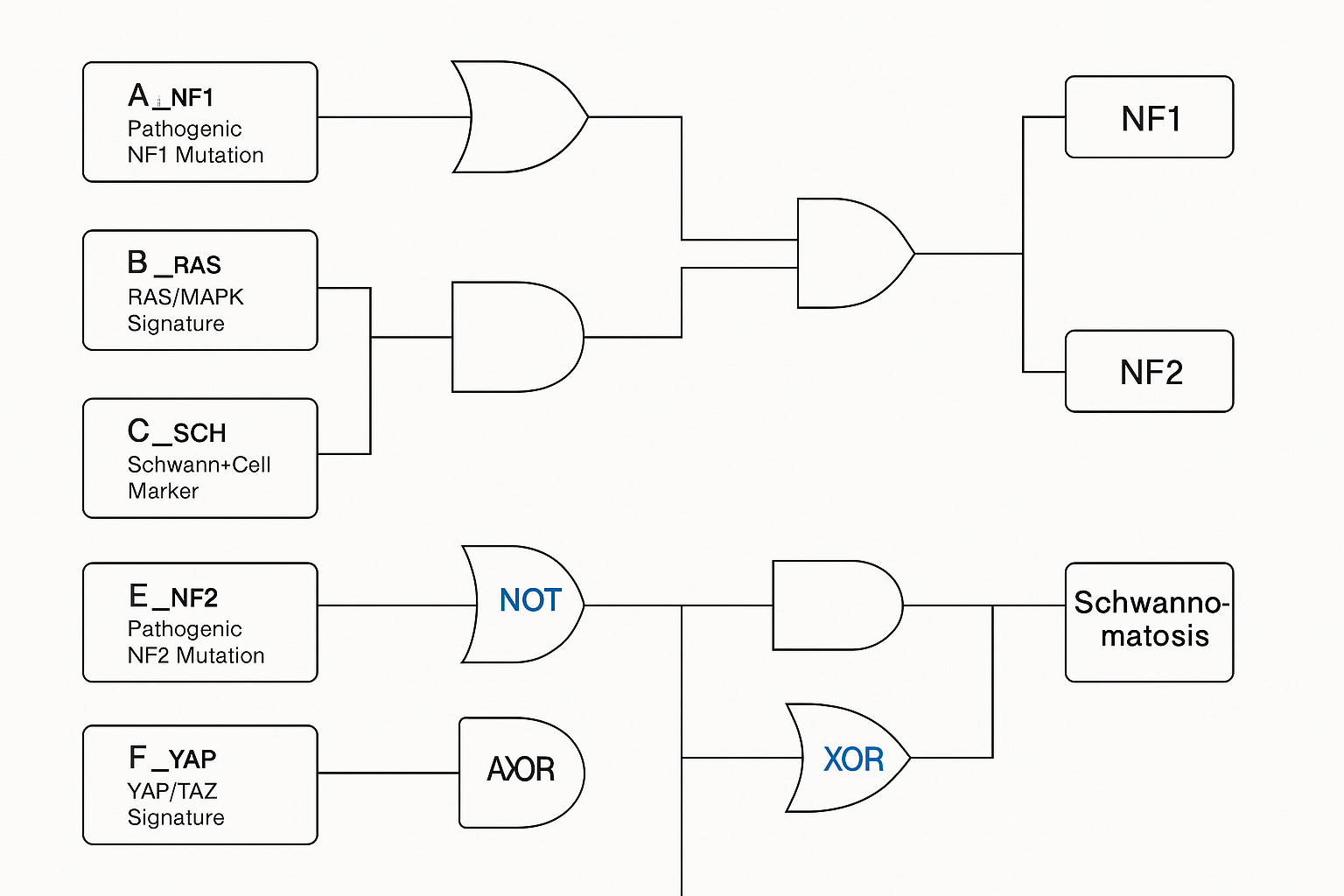
Logika rozstrzygania
-
NF1-POS = A_NF1 OR ( B_RAS AND NOT E_NF2 AND NOT (G_SMARCB1 OR H_LZTR1) )
-
NF2-POS = E_NF2 AND ( F_YAP OR C_SCH ) AND NOT A_NF1
-
SCH-POS (NF3) = ( (G_SMARCB1 XOR H_LZTR1) AND C_SCH ) AND NOT E_NF2 AND NOT A_NF1
Mini „tabela prawdy” (uproszczona, kluczowe wejścia)
| A_NF1 | E_NF2 | (G∨H) | B_RAS | F_YAP | C_SCH | Wynik |
|---|---|---|---|---|---|---|
| 1 | 0 | 0 | 1/0 | x | x | NF1 |
| 0 | 1 | 0 | x | 1 | 1/0 | NF2 |
| 0 | 0 | 1 | x | x | 1 | Schwannomatoza (NF3) |
| 0 | 0 | 0 | 0 | 0 | x | Negatywny / inny |
x – nieważne dla decyzji; 1/0 – akceptuje obie wartości.
Jak to „zrobić w probówce” (warianty)
-
CRISPR-diag (Cas12/13): dla każdego wejścia sonda + reporter fluorescencyjny; sygnały łączone kaskadą AND/OR/NOT (np. bramki NOR/NAND przez cięcie blokad).
-
Toehold switches (RNA): bramki AND szeregowo w 5’UTR reportera; NOT przez konkurencyjny toehold.
-
DNA strand displacement: kaskady wypierania nici jako czysta chemia DNA (bez białek), proste AND/NAND/XOR.
Praktyczne wskazówki
-
Panel mutacji: NF1/NF2 są heterogeniczne → użyj biblioteki sond (hotspoty + sondy na „indel-junction”).
-
Materiał: krew (cfDNA/cfRNA), wymaz policzkowy (germline), lub bioptat guza (dla C_SCH/F_YAP).
-
Kontrola: kanał wewnętrzny RNase P / housekeeping; próg decyzyjny ustaw na stosunek sygnałów (TRUE/FALSE) ≥ 10–20×.